La estructura atomica
|
Agregado: 10 de OCTUBRE de 2002 (Por ) | Palabras: 3492 | Votar |
 | Promedio: 9
| Promedio: 9
Categoría: Apuntes y Monografías > Química >
Material educativo de Alipso relacionado con estructura atomica
Enlaces externos relacionados con estructura atomica
Estructura Atómica
El átomo está formado por un núcleo, que es la masa central de un átomo cargada positivamente, alrededor de la cual se encuentran los electrones orbitales. El núcleo está compuesto por los llamados nucleones (protones y neutrones) y contiene casi toda la masa del átomo.
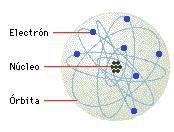
* Los protones son partículas cargadas positivamente cuyo símbolo es p+.
* Los neutrones tienen una carga neutra y se los representa con: no.
* Finalmente los electrones se encuentran girando alrededor del núcleo en orbitales y tienen una carga negativa, su símbolo es e-.
Naturaleza de la Luz
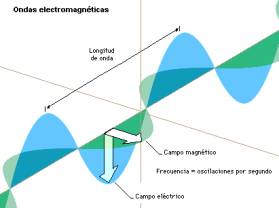
La luz es una onda electromagnética,
constituida por un campo magnético y otro electromagnético que vibran, o
oscilan perpendicularmente entre si.
* La distancia entre unas crestas adyacentes de una onda se llama longitud de onda ( l ).
* El número de veces que una onda oscila en un segundo se denomina frecuencia ( n ).
* La Amplitud está relacionada con la intensidad de las ondas luminosas ( A ).
A veces la luz se comporta mas como una partícula, que como una onda, especialmente cuando interacciona con los átomos. Un átomo siempre absorbe una cantidad determinada de energía o quantum de energía luminosa. Como la interacción implica una cantidad de energía fija, deducimos que la luz se comporta como una partícula denominada fotón. Midiendo la frecuencia de los fotones los científicos pueden determinar que tipo de átomos los emitieron y si proceden de la tierra, el sol o de galaxias lejanas.

La definición de la naturaleza de la luz siempre ha sido un problema fundamental de la física. El matemático y físico británico Isaac Newton describió la luz como una emisión de partículas, y el astrónomo, matemático y físico holandés Christiaan Huygens desarrolló la teoría de que la luz se desplaza con un movimiento ondulatorio.
En la actualidad se cree que estas dos teorías son complementarias, y el desarrollo de la teoría cuántica ha llevado al reconocimiento de que en algunos experimentos la luz se comporta como una corriente de partículas y en otros como una onda. En las situaciones en que la luz presenta movimiento ondulatorio, la onda vibra perpendicular a la dirección de propagación; por eso, la luz puede polarizarse en dos ondas perpendiculares entre sí.
Espectro Electromagnético

La luz visible solo representa una parte muy estrecha del espectro electromagnético, que incluye muchos tipos de ondas.
Espectros Atómicos
Si un átomo absorbe energía está en un estado excitado en relación a su estado normal o fundamental al que trata de regresar devolviendo la energía recibida.
Al hacerlo, emite luz que es de un color característico para cada átomo. Cuando la luz de estos átomos excitados se ve a través de un espectroscopio, se tiene un espectro de rayas o discontinuo. El espectroscopio es un aparato que descompone la luz en sus componentes.
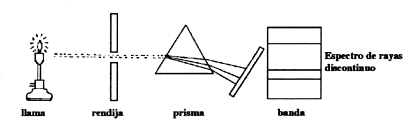
El espectro de este átomo es discontinuo, ósea que está formado por una serie de rayas cuya complejidad depende del número de electrones que posee el átomo. Para el hidrogeno cuyo espectro atómico es el más sencillo se observan varias rayas en la región visible, aunque tiene también otras líneas en el infrarrojo y en la ultravioleta
Si se calienta un metal, producirá luz visible que de pende de la temperatura a la que se encuentra (roja oscura, roja blanquecina, violeta). El pirómetro óptico emplea esta propiedad para medir la temperatura. Si se examina esta luz con un espectroscopio se observa un espectro continuo que contiene luz de todas las longitudes de onda.
La luz blanca emitida por un filamento incandescente produce también un espectro continuo

El espectro discontinuo (de rayas o de líneas) de cada elemento, es tan característico, que se emplea para la identificación de dicho elemento.
Para el hidrogeno, el espectro visible es bastante sencillo, pues consta de una línea roja, una verde y varias azules y violetas que parecen convergir hacia un límite en la región ultravioleta.

En 1885 Balmer demostró que éstas líneas espectrales se pueden expresar con la ecuación:
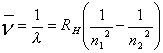
l = longitud de onda de la línea espectral.
n-- = es recíproco de la longitud de onda (número de onda).
RH es la constante da Rydberg (109.678 cm-1)
n es un número entero mayor que 2 (según Balmer).
La ecuación anterior se puede generalizar para las otras líneas del espectro atómico del H.
Modelos Atómicos
Los diferentes experimentos señalados antes, indicaban que los átomos son partículas cuya compleja estructura detallada se explicaba con los denominados "modelos atómicos" propuestos por diferentes científicos en base a los resultados de nuevos experimentos.
Las primeras ideas de la estructura del átomo fueron enunciadas por Thomson cuando ya se había descubierto el electrón en el año de 1.898, este decía que el átomo era un conjunto esférico de cargas positivas cuyos electrones se encontraban incrustados y distribuidos regularmente dentro del campo positivo. y en un número tal que compensaba la carga positiva del átomo.
Este modelo denominado también de "uvas en gelatina" perdió validez o raíz de los resultados obtenidos por Rutherford, que demostraron la existencia del Núcleo Atómico.
Rutherford propuso un nuevo modelo atómico en el cual colocó al núcleo en el centro del átomo y alrededor de este una nube de electrones los cuales poseían car�ga negativa, en el núcleo se encontraba la mayor parte de la masa y además lo car�ga positiva del átomo
La dimensión del diámetro del átomo es de 10-10 m. mientras que la del núcleo es de 10-14 m. Entonces el átomo es l0.000 veces más grande que el núcleo por lo que la mayor parte del átomo se encuentra vacía.
En 1.9l3 cuando yo se conocía lo suficiente acerco de la naturaleza del Átomo, Bohr propuso el modelo planetario para el átomo de Hidrógeno en al cual enunciaba que el núcleo se encontraba en reposo y que los electrones giraban alrededor de éste en órbitas circulares que podían tener ciertos radios según los postulados que y enunciaron.

Posteriormente se
modificó el modelo de Bohr, al suponer la existencia de órbitas elípticas para
los electrones, como lo propuso Sommerfield, pero este modelo pese a visualizar
una de las imágenes más conocidas y publicitadas del Átomo no se ajustaba
completamente a las observaciones efectuadas.

Teoría de Bohr
En 1911, Rutherford estableció la existencia del núcleo atómico. A partir de los datos experimentales de la dispersión de partículas alfa por núcleos de átomos de oro, supuso que cada átomo está formado por un núcleo denso y con carga positiva, rodeado por electrones cargados negativamente que giran en torno al núcleo como los planetas alrededor del Sol. La teoría electromagnética clásica desarrollada por el físico británico James Clerk Maxwell predecía inequívocamente que un electrón que girara en torno a un núcleo radiaría continuamente energía electromagnética hasta perder toda su energía, y acabaría cayendo en el núcleo. Por tanto, según la teoría clásica, el átomo descrito por Rutherford sería inestable. Esta dificultad llevó al físico danés Niels Bohr a postular, en 1913, que la teoría clásica no es válida en el interior del átomo y que los electrones se desplazan en órbitas fijas. Cada cambio de órbita de un electrón corresponde a la absorción o emisión de un cuanto de radiación.
La aplicación de la teoría de Bohr a átomos con más de un electrón resultó difícil. Las ecuaciones matemáticas para el siguiente átomo más sencillo, el de helio, fueron resueltas durante la segunda y tercera década del siglo XX, pero los resultados no concordaban exactamente con los datos experimentales. Para átomos más complejos sólo pueden obtenerse soluciones aproximadas de las ecuaciones, y se ajustan sólo parcialmente a las observaciones.
La teoría de Bohr cuenta con cuatro postulados que son:
1. El átomo de hidrogeno está compuesto de un núcleo de carga positiva y un electrón de carga negativa que se mueve alrededor del núcleo, en una órbita circular de radio r.
2.
No
son permitidas todas las órbitas circulares para el electrón, solamente se
permiten aquellas que tienen momento angular (mvr) múltiplo de ![]()
3. Como consecuencia de las restricciones para las órbitas de un electrón, se fija la energía de un electrón en una órbita dada. Mientras el electrón se mueve en ésta órbita no absorbe ni emite energía.
4. Para cambiar
de una órbita a otra el electrón debe absorber o emitir energía exactamente
igual a la diferencia de energías entre las órbitas involucradas ene esa
transición electrónica. Si la energía el luminosa y el electrón regresa de la órbita n2 a la órbita n1, el fotón emitido tiene una frecuencia dada
por la expresión: 
Mecánica Ondulatoria
El físico francés Louis Victor de Broglie sugirió en 1924 que, puesto que las ondas electromagnéticas muestran algunas características corpusculares, las partículas también deberían presentar en algunos casos propiedades ondulatorias (Dualidad onda-corpúsculo).
La dualidad de onda corpúsculo es la posesión de propiedades tanto ondulatorias como corpusculares por parte de los objetos subatómicos. El principio fundamental de la teoría cuántica es que una entidad que estamos acostumbrados a considerar como una partícula (por ejemplo, un electrón, con un momento lineal p) puede comportarse también como una onda, mientras que otras entidades que solemos concebir como ondas (por ejemplo, la luz, con una longitud de onda l) también pueden describirse como corpúsculos (en este caso, fotones). La longitud de onda l y el momento lineal p de una entidad cuántica están relacionados por la ecuación pl = h, donde h es una constante conocida como constante de Planck.
Esta dualidad onda-corpúsculo se aprecia especialmente bien en los experimentos de �doble rendija', en los que un cañón de partículas dispara electrones o fotones (uno cada vez) a través de un par de agujeros en una barrera, tras lo que son detectados en una pantalla situada al otro lado. En ambos casos, lo que sale del cañón y lo que llega a la pantalla detectora son partículas, y cada una marca un punto individual en la pantalla. No obstante, la figura global que se acumula en la pantalla a medida que se disparan más y más corpúsculos a través de los dos agujeros es un diagrama de interferencia formado por franjas claras y oscuras, que sólo pueden explicarse como resultado de ondas que pasan por ambos agujeros de la barrera e interfieren entre sí. Esto se expresa en el aforismo de que las entidades cuánticas "viajan como ondas pero llegan como partículas".
Esta predicción de la dualidad onda-corpúsculo fue verificada experimentalmente pocos años después por los físicos estadounidenses Clinton Davisson y Lester Halbert Germer y el físico británico George Paget Thomson, quienes mostraron que un haz de electrones dispersado por un cristal da lugar a una figura de difracción característica de una onda. El concepto ondulatorio de las partículas llevó al físico austríaco Erwin Schr�dinger a desarrollar una �ecuación de onda' para describir las propiedades ondulatorias de una partícula y, más concretamente, el comportamiento ondulatorio del electrón en el átomo de hidrógeno.
Aunque esta ecuación diferencial era continua y proporcionaba soluciones para todos los puntos del espacio, las soluciones permitidas de la ecuación estaban restringidas por ciertas condiciones expresadas por ecuaciones matemáticas llamadas funciones propias o eigenfunciones (del alemán eigen, �propio'). Así, la ecuación de onda de Schr�dinger sólo tenía determinadas soluciones discretas; estas soluciones eran expresiones matemáticas en las que los números cuánticos[1] aparecían como parámetros. La ecuación de Schr�dinger se resolvió para el átomo de hidrógeno y dio resultados que encajaban sustancialmente con la teoría cuántica anterior. Además, tenía solución para el átomo de helio, que la teoría anterior no había logrado explicar de forma adecuada, y también en este caso concordaba con los datos experimentales. Las soluciones de la ecuación de Schr�dinger también indicaban que no podía haber dos electrones que tuvieran sus cuatro números cuánticos iguales, esto es, que estuvieran en el mismo estado energético. Esta regla, que ya había sido establecida empíricamente por Wolfgang Pauli en 1925, se conoce como principio de exclusión.
Ecuación de Onda de Schr�dinger
�Considerando la ecuación de onda de De Broglie, Schr�dinger encontró una ecuación similar a las que describen el movimiento de una onda en una región limi�tada del espacio y que podía aplicarse a los electrones de un átomo.
También consideraba el principio de la incertidumbre señalado anteriormente, lo que le permitió determinar niveles de energía y propiedades ondulatorias del átomo de hidrógeno. Además la ecuación de onda es aplicable a átomos diferentes al H. y a las moléculas. aunque su aplicación matemática es extremadamente compleja. Para un sistema de una partícula, la ecuación es:
![]()
m = masa del electrón (o de la partícula)
E = energía total del electrón
V = energía potencial del electrón
h = constante de Planck
x, y, z= coordenadas de la partícula
y = función de onda
Las soluciones de la ecuación anterior son un conjunto de tres valores (x1, Y1. Z1) que se identifican con los números cuánticos establecidos arbitrariamente con la teoría de Bohr, de modo que las soluciones representarían los "orbitales" o regiones en donde (considerando el principio de Heisemberg). la probabilidad de localizar al electrón es máxima.
Aunque no se ha podido resolver la ecuación para un sistema con tres electrones, se considera que mantiene su validez para cualquier átomo ya que los casos que se encontraron soluciones los resultados se han ajustado perfectamente a los experimentos.
La teoría de la mecánica ondulatoria (modelo mecano-cuántico) constituye lo más avanzado y aceptado dentro de la estructura atómica.
Para ilustrar la imagen mecánica-ondulatoria del electrón en un átomo realicemos un experimento imaginario (imposible) con el átomo de H en el estado base o nor�mal (no excitado). "Tomamos una foto" de un sólo átomo miles de veces, utilizando la misma placa fotográfica para lograr una exposición múltiple.

Los resultados hipotéticos aparecen como
puntos que representan al electrón y han formado una nube o densidad esférica y
simétrica alrededor del núcleo. Esto aclara el concepto de orbital indicado
anteriormente, aunque la forma del orbital no nos diga nada acerca de la
verdadera trayectoria del electrón.
Números Cuánticos
Son valores numéricos que definen las características de los electrones de un átomo. Ya en el segundo postulado de la teoría de Bohr se introduce un entero arbi�trario (n) que se define como un número cuántico. luego se introdujeron otros para tratar de mantener la validez de la teoría de Bohr que no explicaba satisfactoriamente la estructura del átomo de hidrógeno y peor aún la estructura de átomos diferentes al hidrógeno.
Los números cuánticos más importantes son cuatro: Principal (n). Secundario (l). Magnético (m), y de Spin (s).
El Número Cuántico Principal indica el nivel en que se encuentra el electrón, su capa u órbita. n puede tomar valores enteros desde 1 hasta 7.
Su valor define la energía que tiene el electrón en el átomo de hidrógeno. En otros átomos la energía no depende totalmente de n. A mayor n, el electrón tiene mayor energía.
El Número Cuántico Secundario indica la existencia de varios subniveles den�tro del mismo nivel (subcapas o subórbitas). Depende del Número Cuántico Prin�cipal y toma valores desde O hasta n - 1.
Se acostumbra sin embargo a utilizar una letra para designar a este número cuán�tico secundario de acuerdo a la siguiente equivalencia:
|
0 |
� |
s (sharp) |
|
1 |
� |
p (principal) |
|
2 |
� |
d (diffuse) |
|
3 |
� |
f (fundamental) |
A este número cuántico se le denomina también del momento angular e indica la forma geométrica aproximada de la "nube electrónica" asociada con el electrón. Por ejemplo todos los orbitales 5 tienen una forma esférica aunque el n sea diferente.
Número Cuántico Magnético.- Cada subnivel contiene uno o más "orbitales' que están relacionados con este tercer número cuántico. índica las posibles orien�taciones de la nube electrónica cuando sobre el átomo actúa un campo magnético externo. Sus valores depende de 1 y van desde - 1 hasta + 1.
Los tres primeros números cuánticos sirven para definir un orbital. Si los elec�trones tienen iguales valores de n, 1 y m, se dice que están en un mismo orbital en el que pueden existir máximo dos electrones según el "Principio de Exclusión de Paulin"
Número Cuántico Spin.- Existe un cuarto número cuántico denominado de Spin que indica el sentido de rotación que tiene n electrón alrededor de su propio eje. Es independiente de los números cuánticos anteriores y toma dos valores + � y - � dependiendo de la dirección de rotación del electrón alrededor de su propio eje.
Configuraciones Electrónicas de los Atomos
La configuración electrónica es una forma resumida de señalar los números cuánticos que tienen los electrones de un átomo. ya que al señalar por ejemplo:
3s2 3 es la capa o nivel (n = 3)
5 es el subnivel (l = 0)
2 es el número de electrones que hay en el subnivel 3s
Las reglas estudiadas anteriormente para los números cuánticos determinan la capacidad de los orbitales, subniveles y niveles ya que:
* cada nivel contiene n subniveles
* cada subnivel contiene 2l + 1 orbitales.
* cada orbital contiene 2 electrones
Para dar las configuraciones electrónicas de los átomos de debe tomar en cuen�ta el llenado de los electrones en el átomo.
En cada átomo los electrones que rodean al núcleo en número igual al número atómico del átomo del elemento; se disponen en los distintos orbitales de acuerdo al "Principio de Exclusión de Pauli" y en orden de sus energías crecientes Regla n+1 o Regla de las Diagonales.
Se llenan primero los orbitales de menor energía para luego ocupar los de energía superior. Puesto que los valores de n y 1 son los únicos que influyen en la energía electrónica entonces la configuración se realiza sin tomar en cuenta los valores de m (número cuántico magnético).
Principio de Exclusión de Pauli
"En un mismo átomo no pueden existir dos electrones que tengan exactamente iguales sus cuatro números cuánticos."
De aquí se deduce que en un orbital (iguales valores de n, 1, y m) existirá un máxi�mo de dos electrones, pues el numero cuántico de spin no puede tomar sino dos posibles valores.
Regla (n + l)
* Los electrones llenan el átomo según su valor creciente de n + l (número cuán�tico principal + número cuántico secundario).
* Cuando dos subniveles tienen el mismo valor de n + 1. se llenará primero el que tiene menor n
* Dentro de cualquier átomo dos electrones se aparean cuando sus números cuán�ticos n, 1 y m son idénticos y sus números cuánticos de spin son diferentes ( + � y - � )
* Como consecuencia de lo anterior se tendrá el siguiente orden de llenado de los electrones.
1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d, 7p.
Regla de Hund
Cuando se llenan orbitales de igual energía (un mismo subnivel) los electrones permanecen en lo posible sin aparearse, es decir que primero entrarán con el mismo spin (por convenio + � ) hasta que se llene la mitad del subnivel, y luego entran con spin opuesto en forma ordenada. (- � ).
Para aplicar esta regla se recurre al denominado diagrama de orbital en el que se indican los números cuánticos m y s luego de la configuración electrónica.
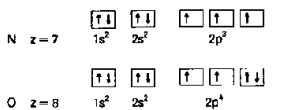
Como corolario de la regla de Hund se tiene "que los subniveles d a medio llenar o completamente llenos ofrecen mayor estabilidad". Esto explica las configu�raciones electrónicas del Cr (Z = 24) oro, paladio, plata. cobre. y algunos lantánidos.
[1] Los números cuánticos son números enteros introducidos en la física de partículas para indicar las magnitudes de determinadas cantidades características de las partículas o sistemas
Comentarios de los usuarios
Agregar un comentario:
Aún no hay comentarios para este recurso.
Monografias, Exámenes, Universidades, Terciarios, Carreras, Cursos, Donde Estudiar, Que Estudiar y más: Desde 1999 brindamos a los estudiantes y docentes un lugar para publicar contenido educativo y nutrirse del conocimiento.
Contacto »



